سلام
در این مطلب میخواهیم با هم به جمع بندی نکات شیمی یازدهم از صفحه 28 تا 58 (مطابق با آزمون) و خلاصه نکات که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
| دانشجوی دکتری تخصصی پیوسته بیوتکنولوژی دانشگاه تهران رتبه 111 منطقه دو - کنکور ریاضی 1394 | |
 | دانشجوی مهندسی عمران دانشگاه تهران رتبه 328 منطقه دو - کنکور ریاضی 1398 |
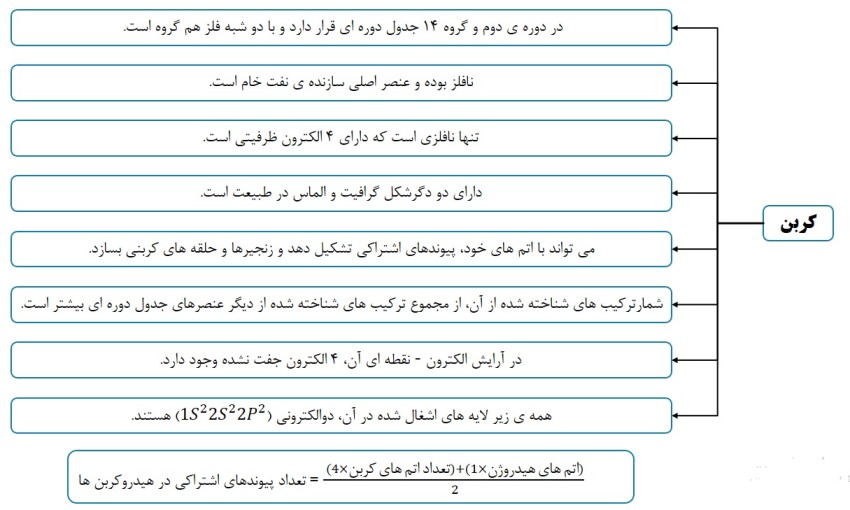
کربن
آلکان ها
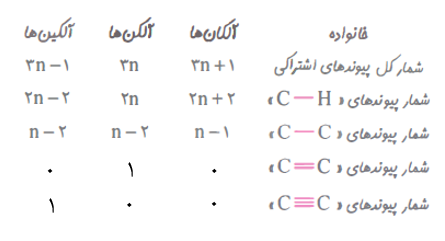
آلکان ها دسته ای از هیدروکربن ها هستند ک در آن ها هر اتم کربن با چهار پیوند یگانه به اتم های اطراف متصل شده است. فرمول عمومی آنها به صورت C(n)H(2n+2) می باشد و جرم مولی آن ها از رابطه 14n+2 به دست می آید.
آلکان ها به دلیل داشتن پیوند های یگانه، تمایلی به انجام واکنش ندارند و سیر شده هستند و گشتاور دو قطبی آن ها حدود صفر است.
آلکان ها هیدورکربن هایی هستند که به دلیل داشتن پیوند های یگانه، تمایلی به انجام واکنش ندارند و سیر شده می باشند. به همین دلیل میزان سمی بودن آن ها کمتر شده و استنشاق آن ها بر شش ها و بدن تاثیر چندانی ندارد و فقط سبب کاهش مقدار اکسیژن در هوای دم می شوند. از این رو هیچ گاه برای برداشتن بنزین از مکیدن شلنگ استفاده نکنید؛ چون بخار های بنزین وارد شش ها شده و از انتقال گاز های تنفسی در شش ها جلوگیری می کند و نفس کشیدن دشوار می شود.
تجربه نشان می دهد که گشتاوردوقطبی آلکان ها حدود صفر است. بنابراین ناقطبی بوده و در آب نامحلول اند.
این ویژگی باعث می شود از آن ها برای حفاظت از فلزها استفاده شود. به این ترتیب که فلزها را در آلکان های مایع قرار می دهند و یا سطح فلزها را با آلکان ها، اندود می کنند تا از خوردگی فلز جلوگیری شود.
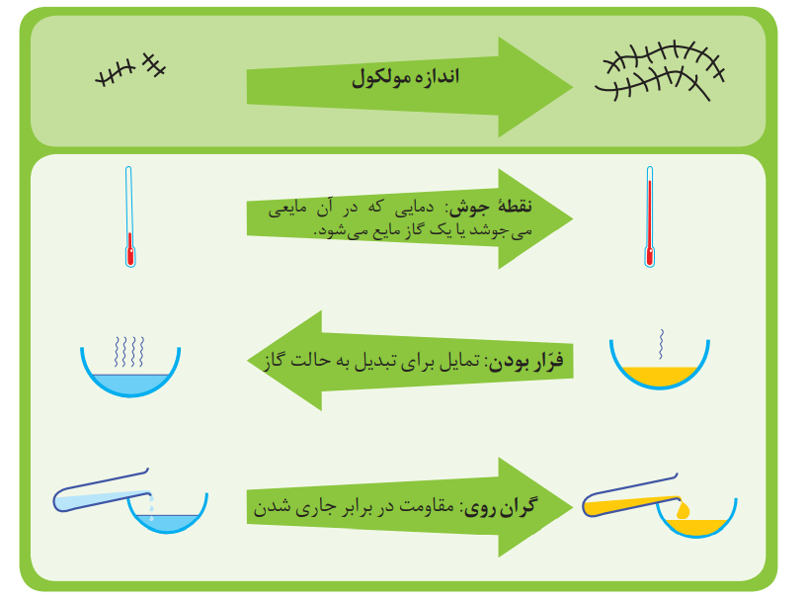
نقطه جوش: به طور کلی با افزایش تعداد اتم های کربن و افزایش جرم مولی آن ها نیروی بین مولکولی که از نوع وان دروالسی است، قوی تر شده و نقطه جوش افزایش می یابد.
فرار بودن: به طور کلی هر چه نقطه جوش پایین تر باشد میزان فرار بودن آلکان ها نیز بیشتر است. بنابراین هر چه تعداد اتم های کربن کمتر باشد(جرم مولی کمتر)، فرار بودن آلکان بیشتراست.
گران روی: به طور کلی هر چه تعداد اتم های کربن در آلکان ها بیشتر باشد، گران روی آلکان نیز بیشتراست.
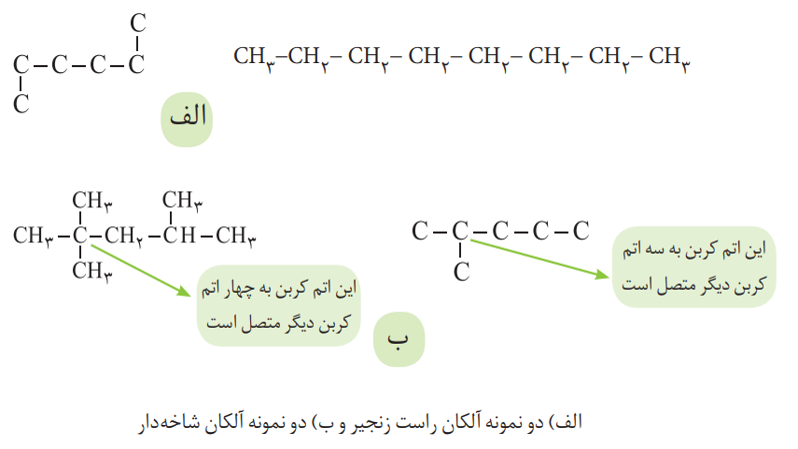
آلکان ها با توجه به نحوه قرار گرفتن اتم های کربن موجود در آن ها به دو دسته زیر تقسیم می شوند:
1- آلکان ها راست زنجیر: در این نوع آلکان ها، هر اتم کربن به یک یا دو اتم کربن دیگر متصل شده است.
2- آلکان های شاخه دار: در این آلکان ها، برخی کربن ها به سه یا چهار اتم کربن دیگر متصل اند.
آلکیل ها: اگر یک اتم H از فرمول آلکان ها کم کنیم گروهی جدیدی به نام آلکیل ها با فرمول CnH2n+1 به دست می آید. مانند متیل(CH3) و اتیل (C2H5)
قواعد نام گذاری آلکان های راست زنجیر:
1- زنجیری که بیش ترین تعداد کربن پشت سر هم را دارد به عنوان زنجیر اصلی انتخاب می کنیم.
2- اگر در مورد یک ترکیب، بتوان دو زنجیر اصلی با تعداد کربن برابر انتخاب کرد، زنجیری را به عنوان زنجیر اصلی انتخاب کنید که تعداد شاخه های فرعی آن بیشتر است.
3- زنجیر اصلی را از سمتی نام گذاری میکنیم که زودتر به شاخه فرعی برسیم.
4- اگر فاصله نخستین شاخه های فرعی در دو سر زنجیر اصلی یکسان باشد، شماره گذاری را از طرفی شروع می کنیم که زودتر به دومین شاخه فرعی برسیم.
5- اگر روی شاخه اصلی چند شاخه فرعی مشابه باشد. ابتدا شماره کربن های دارای شاخه، سپس تعداد شاخه های فرعی را با اعداد یونانی(دی، تری، تترا، پنتا ...) بیان و در آخر نام شاخه فرعی را می نویسیم.
6- در نام گذاری ابتدا نام شاخه فرعی را می آوریم که اولین حرف آن در زبان انگلیسی مقدم تر باشد. به عنوان مثال اتیل زودتر از متیل می آید.
7- اگر شاخه فرعی به جای گروه های آلکیل، هالوژن باشد، نام آن با پسوند (و) می آید؛ به عنوان مثال: Cl کلرو یا Br برمو
8- در انتخاب زنجیر اصلی دقت کنیم که گروه اتیل نمی تواند در جایگاه دوم قرار بگیرد.
تست 1:

تست 2:

آلکن ها
این هیدروکربن ها در ساختار خود دارای پیوند دوگانه کربن – کربن هستند. فرمول عمومی آن ها به صورت C(n) H(2n) می باشد و جرم مولی آن ها از رابطه 14n به دست می آید. ساده ترین آلکن دارای ( 2=n) می باشد. پس دارای فرمول C(2)H(4) و نام اتن است.
این ماده در بیش تر گیاهان وجود دارد. موز و گوجه فرنگی رسیده گاز اتن آزاد می کنند که موجب سریع تر رسیدن میوه های نارس می شود. به همین دلیل در کشاورزی از گاز اتن به عنوان «عمل آورنده» استفاده می شود.
نام گذاری آلکن های راست زنجیر
در آلکن های راست زنجیر دارای 4 اتم کربن یا بیش تر، پیوند دوگانه می تواند در موقعیت های متفاوتی قرار گیرد. به همین دلیل آلکن مورد نظر از سمت نزدیک تر به پیوند دوگانه شماره گذاری می شود و محل پیوند دوگانه با شماره نخستین کربنی که به پیوند دوگانه متصل است مشخص می شود. سپس قبل از آلکن مورد نظر شماره کربن دارای پیوند دوگانه آورده می شود.
آلکن ها به دلیل داشتن پیوند دوگانه سیر نشده هستند چون هر یک از دو اتم کربن مربوط به پیوند دوگانه به 3 اتم متصل هستند. آلکن ها از آلکان های هم کربن خود، دو اتم هیدروژن کم تر دارند. وجود پیوند دوگانه باعث می شود که رفتار آلکن ها با آلکان ها تفاوت زیادی داشته باشد. به گونه ای که آلکن ها برخلاف آلکان ها واکنش پذیری بیش تری دارند و در واکنش های زیادی شرکت دارند که در صفحه ی بعد اشاره شده است.
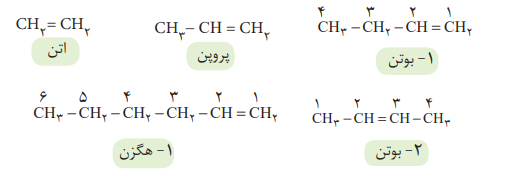
نام و ساختار چند آلکان راست زنجیر
الف) واکنش آلکن ها با آب: در این واکنش الکل تولید می شود. به عنوان مثال با وارد کردن گاز اتن در مخلوط آب و اسید در شرایط مناسب، اتانول (الکل دو کربنه) در مقیاس صنعتی تولید می شود.
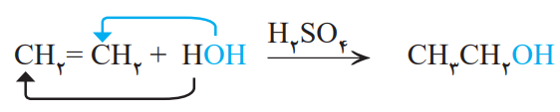
توجه: در این واکنش پیوند کربن – کربن در مولکول اتن شکسته شده و به یکی از کربن ها، اتم H و به دیگری، گروه OH متصل است. در واقع مولکول آب به اتم های کربن اضافه شده و فرآورده سیر شده ای تولید می کند.
نکته: اتانول الکلی بی رنگ و فرار است که به هر نسبتی در آب حل می شود. یکی از مهم ترین حلال های صنعتی است که در تهیه مواد دارویی، آرایشی و بهداشتی به کار می رود. از اتانول در بیمارستان ها به عنوان ضد عفونی کننده استفاده می شود.
ب) واکنش آلکن ها با برم مایع: در این واکنش، پیوند دوگانه میان کربن ها شکسته و دو پیوند جدید بین اتم های کربن و اتم های کربن و اتم های Br (برم) ایجاد می شود. به عنوان مثال بر اثر واکنش برم مایع با گاز اتن، ترکیب سیر شده 2،1- دی برومو اتان به دست می آید.
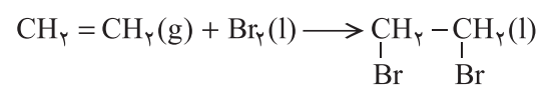
نکته: در این واکنش، رنگ قرمز برم از بین می رود به همین دلیل از این واکنش ها برای شناسایی آلکن ها و اثبات وجود پیوند دوگانه (C = C) استفاده می شود.
نکته: از واکنش تکه ای گوشت چرب با بخار برم، ظرف دارای گاز برم بی رنگ می شود که این امر نشان دهنده سیر نشده بودن چربی است.
پ) پلیمر شدن آلکان ها: این واکنش ها در فصل سوم مورد بررسی قرار می گیرند که برای تولید انواع لاستیک ها، پلاستیک ها و الیاف به کار می رود.
ت) واکنش آلکن با گاز هیدروژن: در این واکنش آلکن ها با گاز هیدروژن(H_2) در حضور کاتالیزگر نیکل (Ni) واکنش داده و به آلکان تبدیل می شود. مانند:
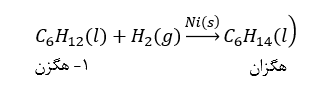
آلکین ها
هیدروکربن های سیر نشده ای هستند که در ساختار خود یک پیوند سه گانه کربن-کربن(C≡C) دارند. فرمول عمومی آن ها به صورت C(n) H(2n-2) می باشد. که در آن ها ...و n=1,2,3 است. جرم مولی آن ها از رابطه 14n-2 به دست می آید.
ساده ترین آن ها اتین (C2H2) است و برای نام گذاری سایر آن هامانند آلکن ها عمل می شود.بااین تفاوت که انتهای نام زنجیر اصلی از پسوند «ین» به جای « ِ ن» استفاده می شود.
آلکین ها از آلکان های هم کربن، 4 اتم هیدروژن کم تر و از آلکن های هم کربن، 2 اتم هیدروژن کم تر دارند. پس سیر نشده محسوب می شوند. البته واکنش پذیری آن ها از آلکن ها بیش تر است، چون سیر نشده تر از آلکن ها هستند.
آلکان < آلکن < آلکین :واکنش پذیری
هیدرو کربن های حلقوی
ترکیب های آلی بسیاری شناخته شده اند که در آن ها از اتصال 3 کربن، ساختاری حلقوی به وجود می آید.
هیدروکربن های حلقوی می توانند سیر شده یا سیر نشده باشند. به عنوان مثال سیکلو آلکان ها، سیرشده و ترکیبات آروماتیک سیر نشده می باشند.
سیکلو آلکان ها: هیدروکربن های حلقوی سیر شده ای هستند که فرمول عمومی آن ها C(n) H(2n) می باشد. در آن ها ... و 4 و 3= n است.
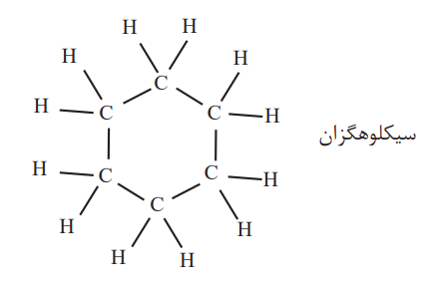
هیدروکربن های آروماتیک: هیدروکربن های حلقوی سیر نشده ای هستند که بنزن (C6H6) سرگروه آن ها می باشد و دارای ساختار زیر است.
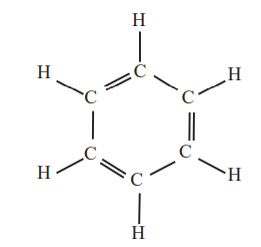
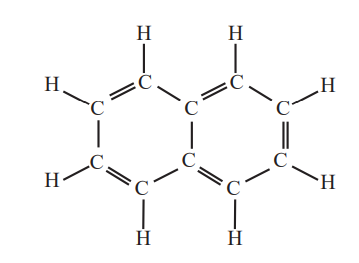
نفتالن: یکی دیگر از ترکیبات آروماتیک است که دارای فرمول مولکولی (C10H8) می باشد. در این ترکیب پنج پیوند دوگانه یکی در میان و دو حلقه شش ضلعی وجود دارد.
نفت
پس ازجداکردن نمک ها، اسید ها و آب، نفت خام را پالایش می کنند. برای این کار از تقطیر جزء به جزء استفاده می شود. طی آن نفت خام را درون محفظه ای بزرگ گرما می دهند و آن را به برج تقطیر هدایت می کنند. درون برج تقطیر دما از پایین به بالا کاهش می یابد. بنابراین هنگامی که نفت خام داغ وارد قسمت پایین برج می شود، مولکول های سبک تر و فراتر (مانند مواد پتروشیمیایی) از مایع بیرون آمده و به سوی بالای برج حرکت می کنند. به تدریچ که این مولکول ها بالاتر می روند سرد شده و به مایع تبدیل می شوند و در سینی هایی که در فاصله های گوناگون برج قرار دارند وارد شده و از برج خارج می شوند. بنابراین محفظه هایی با نقطه جوش نزدیک به هم از نفت خام جداسازی می شوند که این مخلوط ها عبارت است از بنزین و خوراک پتروشیمیایی، نفت سفید، گازوییل، نفت کوره و ...
مقایسه اندازه مولکول ها: نفت کوره > گازوییل > نفت سفید > بنزین و خوراک پتروشیمی
نکته: هر چه درصد فراوانی بنزین و خوراک پتروشیمی در گونه ای از نفت بیش تر باشد، ارزش و کاربرد بیش تری دارد. به همین دلیل قیمت نفت برنت دریای شمال در مقایسه با سایر نفت ها بیش تر است و قیمت نفت سنگین کشور های عربی از دیگر نفت ها کم تر است.
تست 3:

تست 4:

غذا و ارتباط آن با دما، گرما و انرژی
نقش غذا در بدن علاوه بر رفع گرسنگی به صورت زیر است:
1- تامین انرژی مورد نیاز برای حرکت ماهیچه ها، ارسال پیام عصبی، جا به جایی یون ها و مولکولها از دیواره ی سلولی
2- ماده ی اولیه برای ساخت و رشد بخش های گوناگون بدن مانند سلول های خونی، استخوان، پوست، مو، ماهیچه ها، آنزیم ها و...
نکته: هر ماده ی غذایی انرژی دارد و میزان آن به جرمی که می سوزد بستگی دارد. این انرژی می تواند باعث تغییر دما شود.
دمای ماده از چه خبر می دهد؟
دما کمیتی است که میزان گرمی و سردی مواد را نشان می دهد. از دیدگاه ذره ای، ذره های سازنده ی ماده همواره در حال جنب و جوش هستند. اما در حالت های فیزیکی متفاوت، میزان جنبش ذرات متفاوت از یکدیگر است.
نکته: به طور کلی این جنبش های نامنظم در حالت گاز شدیدتر از مایع و در حالت مایع نیز شدیدتر از حالت جامد است.
در ضمن هر چه دما بالاتر می رود، این جنبش ها شدیدتر می شود. به همین دلیل بوی غذای گرم آسان تر و سریع تر از غذای سرد به مشام می رسد.
نکته:«دمای یک ماده معیاری برای توصیف میانگین تندی و میانگین انرژی جنبشی ذرات سازنده آن است.»
نکته: در دمای معین یک ویژگی مشترک مواد با هر حالتی، وجود جنبش های نامنظم ذرات سازنده ی آن هاست و هر چه دمای ماده بالاتر رود، میانگین تندی و میانگین انرژی جنبشی ذرات بیشتر است.
مجموع انرژی جنبشی ذرات سازنده ی یک نمونه ماده را انرژی گرمایی آن ماده می گویند. انرژی گرمایی، به دما و تعداد ذره های سازنده ی ماده (جرم ماده) وابسته است. به این ترتیب که هر چه دما و جرم جسمی بیشتر باشد، انرژی گرمایی آن نیز بیشتر است.
یکای رایج دما، درجه ی سلسیوس (℃) است، در حالی که یکای دما در «SI» کلوین (K) است. البته ارزش دمایی (1℃) برابر با (1K) است. از این رو در فرآیند هایی که دما تغییر می کند، ∆θ=∆T خواهد بود.
تفاوت دما و گرما
به طور کلی به مقدار انرژی گرمایی که به دلیل تفاوت در دما جاری می شود گرما گفته می شود که با نماد (Q) نشان داده می شود و یکای اندازه گیری آن در «SI» ژول (J) است. البته هنوز در برخی موارد از کالری (cal) برای بیان مقدار گرما استفاده می شود.
ایستگاه محاسبات cal=4.18 J
به مقدار گرمای لازم برای افزایش دمای یک جسم به اندازه ی (1℃) ظرفیت گرمایی آن جسم گفته می شود که با حرف (C) نمایش داده می شود. Q=C∆θ
نکته: ظرفیت گرمایی یک ماده در دما و فشار ثابت به نوع ماده و مقدار آن بستگی دارد. بنابراین هر چه جسمی بیش تر باشد، ظرفیت گرمایی آن نیز بیشتر است.
به مقدار گرمای لازم برای افزایش دمای یک گرم از یک جسم به اندازه ی (1℃) ظرفیت گرمایی ویژه آن جسم گفته می شود که با حرف (c) نمایش داده می شود. Q=mc∆θ
دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
با آرزوی موفقیت و کامیابی


