سلام
در این مطلب میخواهیم با هم به جمع بندی نکات ساختار لوویس و قانون گازها (مطابق با آزمون جامع) و خلاصه نکات که برای پاسخگویی به سوالات آزمون باید به آنها مسلط باشید، بپردازیم.
رسم ساختار لوویس
برای رسم انواع ساختار لوویس از الگوریتم داده شده استفاده میکنیم مراحل باید به ترتیب طی شوند.
1-مجموع تعداد الکترون های ظرفیت اتم های موجود در مولکول را محاسبه کنید.
2-تعداد الکترون های لازم برای هشتایی شدن را به صورت زیر محاسبه کنید.
3-
4- اتمی که در فرمول شیمیایی ترکیب مورد نظر در سمت چپ نوشته می شود را (به جز اتم H) به عنوان اتم مرکزی انتخاب کنید.
5-اتم های اطراف را با استفاده از تعداد پیوند های به دست آمده در مرحله ی سوم به اتم مرکزی متصل کنید.
نکته: اتم های هیدروژن و هالوژن ها با پیوند یگانه به اتم مرکزی وصل می شوند.
نکته: اتم های اکسیژن و گوگرد می توانند در صورت نیاز با پیوند دوگانه به اتم مرکزی متصل شوند.
نکته: اتم نیتروژن می تواند با پیوند سه گانه به اتم مرکزی متصل شود.
6-در اطراف (به جز اتم H) به تعداد مورد نیاز برای هشتایی شدن، الکترون ناپیوندی قرار دهید.
برای بدست آوردن بار یون ها، در صورتی که تعداد ساختار لوویس آن داده شده باشد، می توانید از رابطه مقابل استفاده کنید:

باران اسیدی
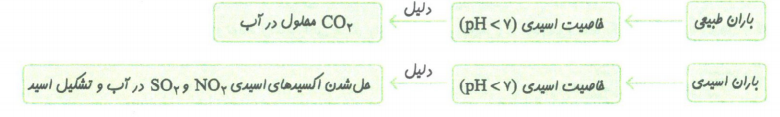
باران طبیعی به دلیل وجود کربن دی اکسید محلول در آن، اندکی اسیدی و دارای pH کمتر از ۷ است، اما برخی آلاینده های هوا مانند NO,SO که اکسید اسیدی هستند، می توانند با آب و اکسیژن موجود در هوا واکنش دهند و در نهایت به اسیدهای قوی نیتریک اسید و سولفوریک اسید تبدیل شوند.
این اسیدها به طور قابل توجهی! بر مقدار اسیدی بودن آب باران اضافه می کنند. به این باران، باران اسیدی می گویند. و باران اسیدی آثار جبران ناپذیری بر جنگل ها، باغ های میوه و زندگی آبزیان دارد. هم چنین آثار زیان بار باران اسیدی بر روی پوست، دستگاه تنفس و چشم ها به سرعت قابل تشخیص است و گاهی خاصیت اسیدی آن باعث خشک شدن و ترک خوردگی پوست بدن می شود.




خواص و رفتار گازها:
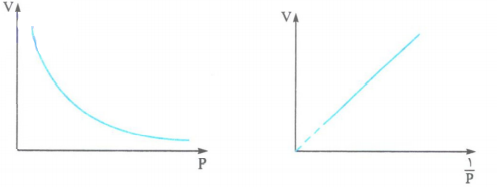
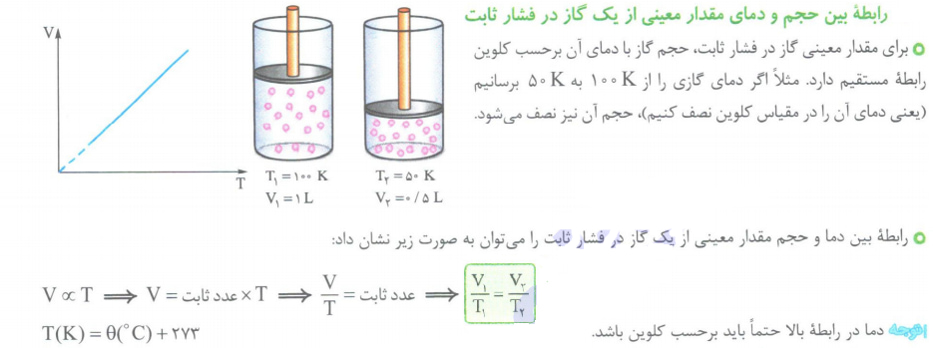
1- رابطه بین فشار و حجم گاز:
به طور کلی برای مقدار مشخصی گاز در دمای ثابت، حجم گاز با فشار آن رابطه عکس دارد.(قانون بویل)
به عنوان مثال اگر فشار وارده بر یک گاز دو برابر شود، حجم آن نصف شده و اگر فشار وارده سه برابر شود، حجم آن یک سوم حجم اولیه می شود.

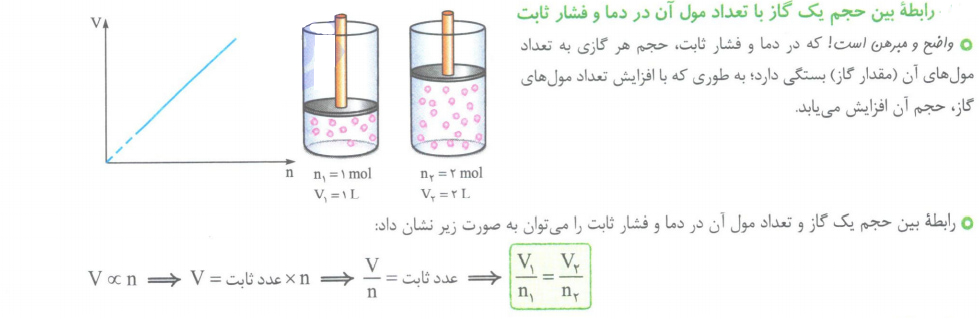


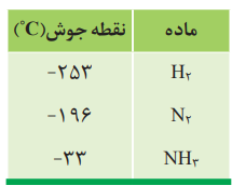
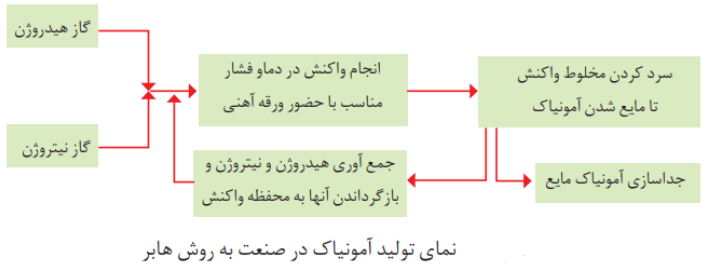
فرآیند هابر
هابر واكنش میان گازهای هیدروژن و نیتروژن را بارها در دماها و فشارهای گوناگون انجام داد تا بتواند شرایط بهینه آن راپیدا كند. سرانجام دریافت که اگر مخلوط این گازها از روی یك ورقه ی آهنی (کاتالیزگر) در دما و فشار مناسب عبور داده شود با انجام واكنش، مقدار قابل توجهی آمونیاك تولید می شود؛ اما همه ی واكنش دهنده ها به فرآورده تبدیل نخواهد شد؛ زیرا این واكنش برگشت پذیر است؛ با این توصیف در ظرف واكنش مخلوطی از سه گاز هیدروژن، نیتروژن و آمونیاك وجود دارد.
تست های منتخب؛ (تست های زیر را حل کنید و پاسخ آن ها را در کامنت ها به اشتراک بگذارید!)
تست 1

تست 2

تست 3

تست 4

تست 5

دوستان عزیز می توانید برای دسترسی به نسخه کامل خلاصه نکات به همراه پاسخ فایل پی دی اف زیر را دانلود کنید!
فراموش نکنید اگر سوالی در رابطه با این مبحث داشتید می توانید به راحتی در کامنت ها سوال خود را برای ما بنویسید.
دوستان عزیزم ما تصمیم گرفتیم برای اینکه بتونیم ارتباطمون رو با هم بیشتر کنیم و قدم به قدم کنارتون باشیم، صفحه ی اینستاگرام متا رو بسازیم
و همراهتون باشیم.
با آرزوی موفقیت و کامیابی
گلنوش بیرانوند، دانشجوی مهندسی شیمی دانشگاه شریف
نوید آرمات، دانشجوی مهندسی عمران دانشگاه تهران


