سلام به دوستان کنکوری 1401😊
امیدوارم همگی حالتون خوب باشه.
این مطلب شامل درسنامه مبحث خوردگی آهن و حفاظت از آهن شیمی دوازدهم هست که توسط خانم هما پرتوانداز، رتبه 226 تجربی و 289 زبان منطقه 2کنکور سراسری 99 و دانشجوی پزشکی دانشگاه علوم پزشکی ایران تهیه شده است.
با ما همراه باشید😄
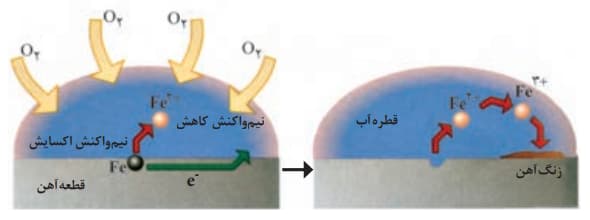
شکل بالا,مربوط به فرآیند زنگ زدن آهن می باشد.
زنگ آهنFe(OH)3 می باشد.در این فرآیند ابتدا Fe+2تشکیل می شود و سپس به Fe+3 تبدیل می شود.
از آنجایی که این فرآیند خود به خود انجام می شود, می توان گفت که مشابه سلول گالوانی عمل می کند.
در بخش کاتدی فرآیند,مولکول های اکسیژن, الکترون های تولید شده از اکسایش آهن را از طریق مولکول های آب جذب می کنند و به یون هیدروکسید(-OH) تبدیل می شوند.
واکنش بخش کاتدی:
در بخش آندی,اتم های آهن به کاتیون Fe+2 و -e تبدیل می شوند. الکترون های تولید شده از طریق خود فلز آهن(رسانای الکترونی) به سمت بخش کاتدی(جایی که میزان O2 زیاد است)مهاجرت می کنند و O2 به-OH تبدیل می شود.
یون های Fe+3 که از قبل تشکیل شده اند,به بخش کاتدی می رسند و با یون های -OH واکنش داده و رسوب Fe(OH)3را تشکیل می دهند.
فلزهای نجیبی مانند طلا و پلاتین حتی در محیط های اسیدی اکسایش نمی یابند اما وسایل آهنی در هوای مرطوب دچار خوردگی می شوند. واکنش ناخواسته ای که در شهرهای بندری و ساحلی بیشتر خودنمایی میکند. بدیهی است که ساده ترین راه برای جلوگیری از خوردگی آهن، ایجاد یک پوشش محافظ است تا از رسیدن اکسیژن و رطوبت به آهن جلوگیری کند. پوششی که با روش هایی مانند رنگ زدن، قیراندود کردن و روکش دادن ایجاد می شود. باید توجه داشت که چنین روش هایی نمیتوانند بهطور کامل از خوردگی پیشگیری کنند زیرا به تدریج رطوبت و اکسیژن از روزنه های این پوشش ها به درون نفوذ کرده و به سطح آهن می رسند و خوردگی دوباره آغاز می شود.
در آهن سفید,هر گاه خراشی ایجاد شود,در محل ایجاد خراش یک سلول گالوانی تشکیل می شود.در این سلول روی به عنوان آند اکسایش می یابد و آهن به عنوان کاتد, حفاظت کاتدی می شود.الکترون های حاصل از اکسایش فلز روی به سطح فلز آهن که بیشتری دارد منتقل می شوند,ولی چون فلزها نمی توانند الکترون بگیرند,فلز آهن الکترون ها را در حضور رطوبت به اکسیژن هوا می دهد.
برای ساخت قوطی مواد غذایی کنسروی از آهن گالوانیزه استفاده نمی شود زیرا روی(Zn) در اسید مواد غذایی حل شده و ماده غذایی مسموم و فاسد می شود.بنابراین از حلبی برای ساختن آنها استفاده می کنند.
شکل زیر بخشی از یک ورقۀ آهنی را نشان میدهد که با لایۀ نازکی از قلع پوشیده شده است. به این نوع آهن، حلبی میگ ویند. از ورقه های حلبی برای ساختن قوطی های روغن نباتی و کنسرو استفاده می شود.
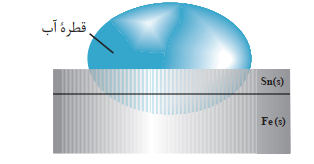 اگر خراشی در سطح حلبی ایجاد شود,در حضور رطوبت یک سلول الکتروشیمیایی تشکیل می شود که آهن با کوچک تر, نقش آند سلول و قلع با بزرگتر, نقش کاتد سلول را خواهد داشت.بنابراین قلع در نقش کاتد,حفاظت می شود و آهن از بین می رود.
اگر خراشی در سطح حلبی ایجاد شود,در حضور رطوبت یک سلول الکتروشیمیایی تشکیل می شود که آهن با کوچک تر, نقش آند سلول و قلع با بزرگتر, نقش کاتد سلول را خواهد داشت.بنابراین قلع در نقش کاتد,حفاظت می شود و آهن از بین می رود.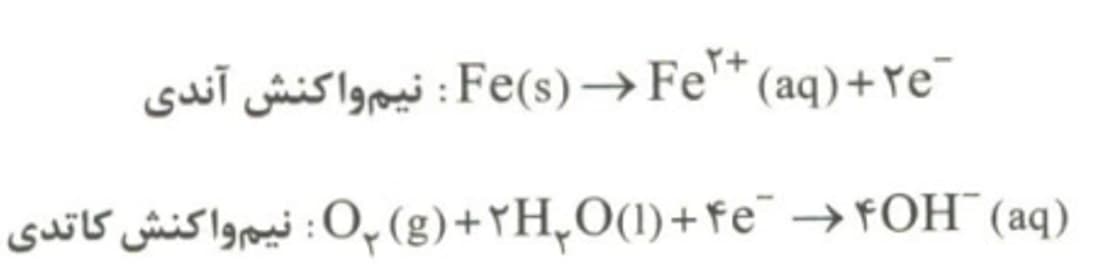
تست ها:
1-


2-


3-

 صفحه اینستاگرام تجربی گروه برترها
صفحه اینستاگرام تجربی گروه برترها
برای رزرو مشاوره و رفع اشکال درسی و شرکت در کلاس های کنکوری با مشاوران سایت برترها، واردسایت برترهاشوید یا با شماره تماس 0216463 داخلی1174(حیدریان) تماس بگیرید.
مطالب دیگر از هماپرتوانداز:


